A genetikai tanácsadás összetett feladat, része az alapos anamnézisfelvétel, a genetikai kockázat felmérése, a megfelelő tesztek lekérése, az eredmények interpretálása a személyes és a családi fenotípus ismeretében, surveillance- vagy rizikófüggő szűrések, valamint a vizsgálatoknak a páciens körülményeihez való igazítása.
A genetikai tanácsadásnak fontos szerepe lehet például egy olyan család esetében, ahol több generáció tagjain előfordul örökletes daganatos szindróma. Az időben végzett genetikai felmérés javíthatja a betegség kimenetelét és a prevencióban is meghatározó jelentőségű. Emellett a genetikai tanácsadás egyre növekvő jelentőséggel bír az eredmények interpretálásban a folyamatosan bővülő molekuláris tesztek piacán.
Az alábbi esettel 2010-ben a City of Hope Rákközpontban foglalkoztam mint genetikai tanácsadó. A 45 éves, latin származású hölgy azt követően került hozzánk, hogy vastagbélrákot diagnosztizáltak nála. Az adenocarcinomát a vastagbél felszálló szárában találták. Az anamnézis felvétele során kiderült, hogy 25 éves korában a bal emlőjében háromszorosan negatív (triple negatív, azaz hormonreceptor-státusában ER-, PR-, her2-negatív) invazív ductalis carcinomát diagnosztizáltak. Harmincéves korában új primer tumort észleltek, ezúttal a tüdejében.
A családi anamnézis részletes felvétele során számos releváns információ derült ki:
– Három házasságából négy gyermeke született. Egyik fia 17 évesen halt meg sikertelenül kezelt glioblastoma miatt. Gyermekének elvesztése óriási lelki traumát okozott betegünknek és lányának is.
– Hetvenéves édesanyja és annak egypetéjű ikertestvére 35 évesen bilateralis mastectomián estek át emlőrák miatt.
– Édesapjánál szintén vastagbélrákot diagnosztizáltak 48 éves korában, és 50 évesen halt meg.
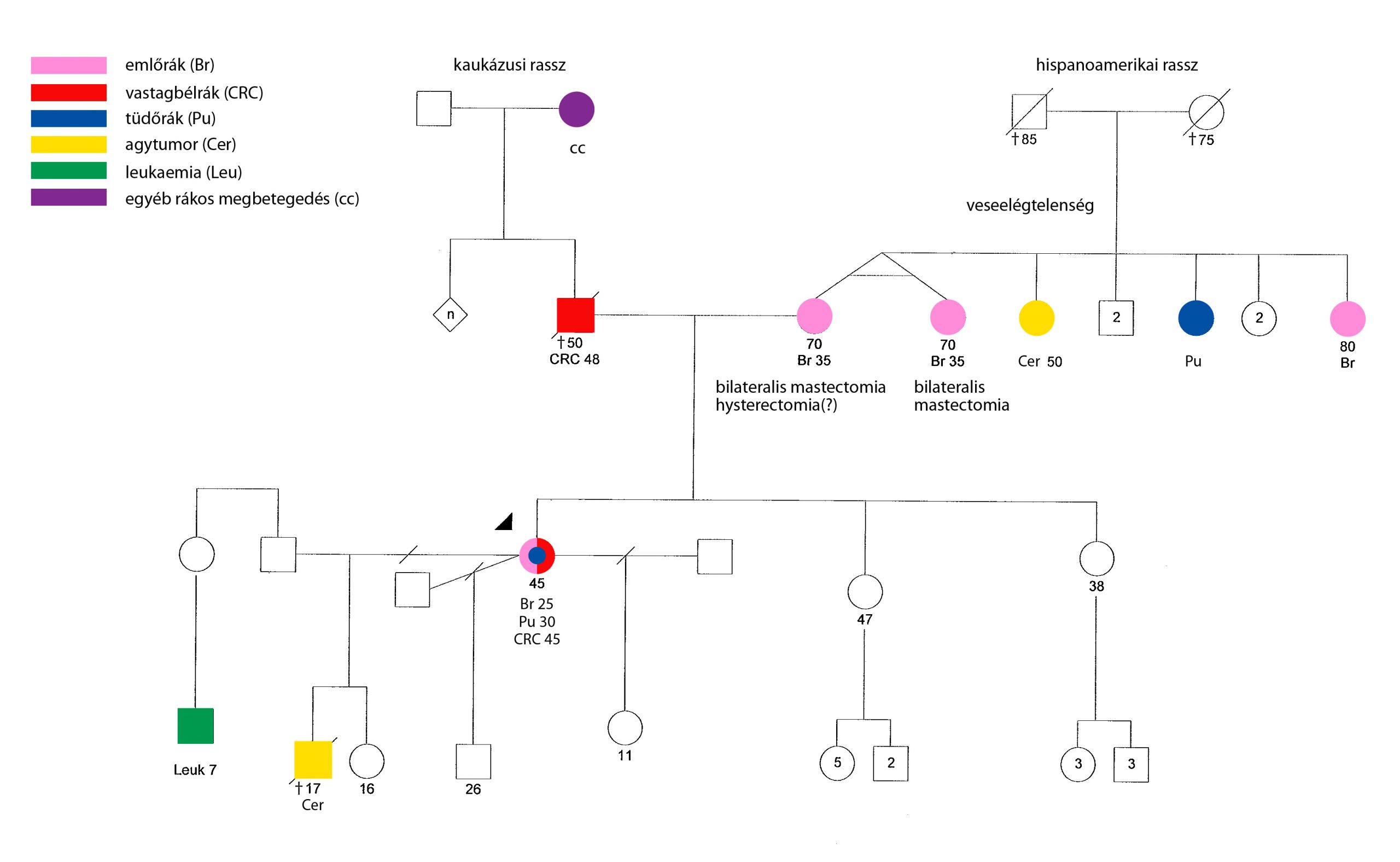
Nagy kérdés volt számomra, hogy miért csak most került hozzánk ez a páciens! Miért kellett megismétlődnie minden intervenció nélkül az előző generációban lezajlottaknak?
A személyes és családfa-kórtörténet alapján több differenciáldiagnosztikai lehetőség volt. A 30 éves kor előtt kezdődő emlőrák önmagában is, de különösen a két további primer daganattal együtt a Li Fraumeni-szindróma (LFS) gyanúját kelti. A páciens fenotípusa a Li Fraumeni-szindróma Chompret-féle klinikai kritériumának felel meg [1].
Ugyanakkor a korai emlődaganat a ritkább, háromszorosan negatív immunfenotípussal a BRCA génekhez kapcsolódó, örökletes emlő- és petefészekrák diagnózis irányába terelt. Ezt az irányt tovább erősíti a családban diagnosztizált korai emlőrák. A BRACAPRO analízis (olyan modell, amivel a családi emlő- és ovariumcarcinoma előfordulásának elemzése alapján a BRCA1- és a BRCA2-mutáció valószínűsége becsülhető meg) eredménye alapján 39%-os kockázata volt a BRCA-mutáció hordozóságára. Ez a számítás még nem vette figyelembe a háromszorosan negatív hormonreceptor-státust, amely a BRCA1-mutáció hordozóságának valószínűségét tovább növelheti [2].
Harmadrészt viszont az 50 éves kor alatti vastagbélrák-diagnózis önmagában megfelel a Bethesda-kritériumnak. A vastagbélrák ugyan része lehet a Li Fraumeni-szindrómának is, az apa coloncarcinoma-diagnózisa miatt a Lynch-szindrómát semmi esetre sem lehetett figyelmen kívül hagyni.
A leírtakból kiderül, hogy a részletes egyéni és családi anamnézis határozott irányt szab a genetikai tanácsadónak a tesztek sorrendjének felállításához, ami összetett feladat. Függ a szindróma valószínűségétől, a negatív prediktív értéktől, a kezelési és a rizikóredukciós beavatkozások lehetőségétől, valamint a rákszűrési stratégia felállításától. Nem elhanyagolható kérdés, hogy ezen vizsgálatok költségeit ki viseli.
A páciens akkori életkörülménye és nem mindenre kiterjedő egészségbiztosítása erőteljesen behatárolta az általunk javasolt genetikai tesztek elvégzésének lehetőségét és sorrendjét.
Kiderítettük, hogy a CMDL laboratórium elfogad mintát a betegtől a Li Fraumeni-szindrómáért felelős P53 gén szekvenálására és nagyobb szakaszt érintő deletioduplikációra, így ezzel kezdtünk. A családban előforduló korai Li Fraumeni-szindróma core-tumorai alapján akár 57% is lehet a mutáció találati valószínűsége [1]. A nagy prediktív kockázat ellenére – a Li Fraumeni-szindrómára jellemző sarcoma core-tumor hiányában – a negatív genetikai eredményt elfogadhatónak és megmagyarázhatónak tartottuk.
A BRCA gének szekvenálását 2010-ben nem fedezte a beteg állami egészségügyi biztosítója, ezért a következő legjobb lehetőséggel élve a latin mutációs panelt végeztük, ami a latin populációban leggyakrabban előforduló ismert mutációkat tartalmazza. A negatív eredmény nem informatív. A BRCA génekben előforduló deletioduplikáció esélye nagyobb a spanyol eredetű populációban, és ennek szűrésére akkor, tudomásom szerint, nem került sor. Ennek értelmében teljesen nem tudtuk kizárni a BRCA-mutáció lehetőségét a családban. A beteg édesanyján és testvérén is megpróbáltuk elvégeztetni a teljes értékű BRCA-tesztet, de ott is falakba ütköztünk.
Ez idő alatt a colontumorból vett mintát az MMR-fehérjék (MLH1, MSH2, MSH6, PMS2) immunohisztokémiai vizsgálatára és mikroszatellitainstabilitás-tesztre küldtük, aminek lelete Lynch-szindrómára utalhat. Az eredmény: MSI-H, azaz instabilitás, illetve MLH1-, PMS2-negatív, azaz fehérjehiány potenciális génhiba miatt. Ez a tumortesztlelet a klinikai képpel együtt diagnosztikus értékű volt. Elvégeztük az MLH1 gén szekvenálását, és informatív eredményt kaptunk: MLH1 c.298C>T p.Arg100X. Ez a kóroki nonsense-pontmutáció magyarázattal szolgál a korai vastagbélrákra.
De hogyan magyarázzuk meg a korai emlőrákot? A mai szakirodalom szerint – bár megoszlik a vélemény – bizonyos Lynch-szindrómás családokban, ha nem is szignifikánsan és ilyen fiatalon, de emelkedett az emlőrák rizikója. Mivel az emlőrák az anyai oldalon jelenik meg, nagy valószínűséggel nincs köze a Lynch-szindrómához.
Miért fontosak az eddigi és a további lépések?
Amennyiben a betegnél egy eddig fel nem fedezett BRCA-mutáció felel az emlőrákért, akkor a megnövekedett kockázat és a hatástalan szűrés miatt erősen ajánlott a rizikóredukciós bilateralis salpingoophorectomia elvégzése. Ez a műtéti beavatkozás azonban az örökletes emlő- és petefészekrák fenotípusa vagy a BRCA-mutáció hiányában nem ajánlott.
Mivel a Lynch-szindróma bizonyítottan fennáll, a vastagbélrák nagyobb kockázata mellett az endometriumcarcinoma (40-60%) és a petefészekrák (10%) kockázata szintén emelkedett. Páciensünk esetében tehát nem elvetendő a totális histerectomia és a bilateralis salpingoophorectomia lehetősége.
Emellett igen fontos gyermekeinek, testvéreinek pontos rizikóelemzése, a rákszűrés tekintetében a személyre szabott ajánlás, valamint a szükséges genetikai tesztek elvégzése 18 éves koruk után.
Irodalom:
1. Gonzalez KD, Noltner KA, Buzin CH, Gu D, Wen-Fong CY, et al. Beyond Li Fraumeni Syndrome: clinical characteristics of families with p53 germline mutations. J Clin Oncol 2009;27(8):1250-6. Epub 2009 Feb 9.
2. Atchley DP, Albarracin CT, Lopez A, Valero V, Amos CI, et al. Clinical and pathologic characteristics of patients with BRCA-positive and BRCA-negative breast cancer. J Clin Oncol 2008;26(26):4282-8.







